![]()
Traducido en la Universitat de València,
España
Tutorial de Química
La Química del Agua
La polaridad del agua|
El agua tiene una estructura molecular simple. Está compuesta por un átomo de oxígeno y dos de hidrógeno. Cada átomo de hidrógeno se encuentra unido covalentemente al oxígeno por medio de un par de electrones de enlace. El oxígeno tiene además dos pares de electrones no enlazantes. De esta manera existen cuatro pares de electrones rodeando al átomo de oxígeno: dos pares formando parte de los enlaces covalentes con los átomos de hidrógeno y dos pares no compartidos en el lado opuesto. El oxígeno es un átomo electronegativo o "amante" de los electrones, a diferencia del hidrógeno. El agua es una molécula "polar"; es decir, existe en ella una distribución
irregular de la densidad electrónica. Por esta razón, el
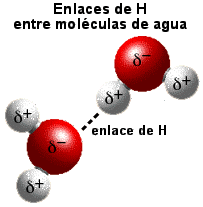
agua posee una carga parcial negativa ( Una atracción electrostática entre la carga parcial positiva cercana a los átomos de hidrógeno y la carga parcial negativa cercana al oxígeno da lugar a un enlace por puente de hidrógeno, como se muestra en la figura. |
|
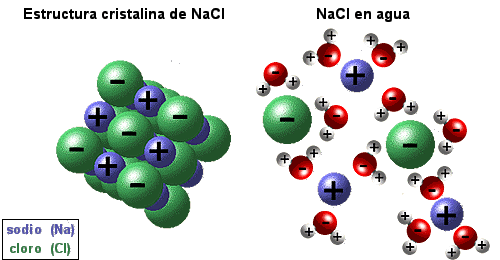
| La habilidad de los iones y otras moléculas para
disolverse en el agua es debida a la polaridad de ésta última. Por ejemplo,
en la imagen inferior se muestra el cloruro sódico en su forma cristalina
y disuelto en agua. |
Muchas otras propiedades únicas del agua son debidas a los
puentes de hidrógeno. Por ejemplo, el hielo flota porque los puentes
de hidrógeno mantienen a las moléculas de agua más
separadas en el agua sólida que en el agua líquida, donde
hay un enlace de hidrógeno menos por cada molécula. Las propiedades
físicas únicas, incluyendo un alto calor de vaporización,
una fuerte tensión superficial, un calor específico alto y
el hecho de ser casi el disolvente universal, también son debidas
a la polaridad del agua y a su capacidad de formar enlaces por puentes de hidrógeno. El efecto hidrofóbico,
o la exclusión de compuestos que contienen carbono e hidrógeno
(sustancias no polares) es otra de las propiedades únicas del agua
causadas por los enlaces de hidrógeno. El efecto hidrofóbico
es particularmente importante en la formación de membranas celulares.
La mejor descripción que puede darse de este efecto es que el agua
"arrincona" a las moléculas no polares, manteniéndolas juntas.
Ácidos y Bases, Ionización del Agua
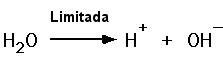
- Los ácidos ceden H+.
- Las bases aceptan H+.
Se define el pH de una disolución como el logaritmo negativo de la concentración de iones de hidrógeno.
- A pH 7.0 la disolución es neutra.
- A un pH menor (1-6) la disolución es ácida.
- A un pH mayor (8-14) la disolución es básica.
Department of Biochemistry and Molecular Biophysics
University of Arizona
Agosto 1996
Revisado: Julio 2005
Traducido: Julio 2005
Contact the Development Team
http://www.biologia.arizona.edu
All contents copyright © 1996-2005. All
rights reserved.
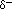 ) cerca del átomo de oxígeno
y una carga parcial positiva (
) cerca del átomo de oxígeno
y una carga parcial positiva (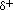 ) cerca de los átomos de hidrógeno.
) cerca de los átomos de hidrógeno.