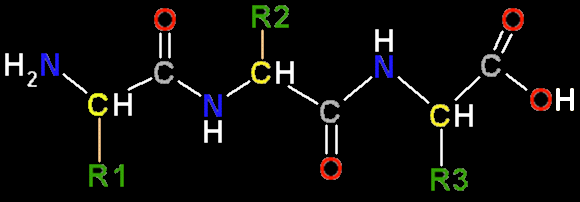
Dois aminoácidos podem se unir covalentemente através duma ligação amida substituída, nomeada ligação peptídica. Esta ligação se forma ao reagir o grupo alfa-carboxilo dum aminoácido com o grupo alfa-amino do outro aminoácido, perdendo-se uma molécula de água. Podem se unir três aminoácidos para formar um tripeptídeo:

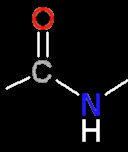
para formar o "esqueleto" do peptídeo.
Neste
modelo de varinhas pode se ver o esqueleto peptídico dum tripeptídeo.
Só estão representados os carbonos
alfa, os átomos que intervém nas duas ligações
peptídicas e os grupos amino e carboxilo terminal. Não se
representam nem as cadeias laterais nem alguns hidrógenios, e do
carboxilo terminal só se representa um dos oxigénios.
Observe como a ligação peptídica é
uma estrutura plana, e como o oxigénio e o hidrogénio
se dispõem em configuração trans.
Agora cada aminoácido tem uma cadeia lateral formada por um carbono. Deste modo temos construído o tripeptídeo Ala-Ala-Ala.
Adicionando um grupo amino e uma cadeia hidrocarbonada a cadeia lateral do aminoácido amino terminal temos o peptídeo Lys-Ala-Ala.
Adicionando mais três carbonos a cadeia lateral do aminoácido carboxilo terminal temos o peptídeo Lys-Ala-Ile.
Podemos adicionar um quarto aminoácido para formar um tetrapeptídeo. Neste caso se tem adicionado o aminoácido treonina para formar o peptídeo Lys-Ala-Ile-Thr. (Identifique o grupo hidroxilo da cadeia lateral da treonina).
Aqui pode se observar a forma do tetrapeptídeo na representação com um modelo espacial. (Observe, mais uma vez , que nem todos os átomos de hidrogénio estão representados).
A representação com modelos de bolas e varinhas proporciona pormenores a mais para representar grandes proteínas. Por essa razão é habitual representar a cadeia peptídica por uma linha que conecta os carbonos alfa de todos os aminoácidos. Essa linha representa o esqueleto do peptídeo.
Se só se mostra o esqueleto peptídico e mais fácil apreciar as estruturas secundária, terciária e quaternária duma proteína.