
|
trifosfato
difosfato
monofosfato
|
 |
|
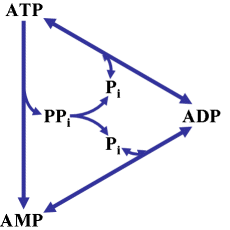
Hay reacciones en las que se hidroliza una molécula de ATP dando una de AMP y otra de PPi. ¿Por qué en estos casos contamos 2 ATP para los balances?
La reacción acoplada es
ATP ![]() AMP + PPi
(rotura de un enlace de elevada energía)
AMP + PPi
(rotura de un enlace de elevada energía)
que va seguida de
PPi ![]() 2 Pi
(rotura de otro enlace de elevada energía)
2 Pi
(rotura de otro enlace de elevada energía)
Es decir, se rompen dos enlaces de elevada energía (fosfoanhídridos)
Visto de otro modo: la célula necesita reciclar ese AMP (nuestro recuento de energía siempre se hace basado en la conversión ATP↔ADP), lo que se consigue fosforilándolo a costa de ATP, así:
AMP + ATP ![]() ADP + ADP
(quinasa del AMP = adenilato quinasa, EC 2.7.4.3)
ADP + ADP
(quinasa del AMP = adenilato quinasa, EC 2.7.4.3)


y al sumar todas las reacciones obtenemos:
2 ATP ![]() 2 ADP + 2 Pi
confirmando la percepción de que se gastan dos unidades de energía
2 ADP + 2 Pi
confirmando la percepción de que se gastan dos unidades de energía
| ruta | enzima | sustrato (A) | intermedio unido a la enzima |
producto (B) |
|---|---|---|---|---|
| ciclo de la urea | argininosuccinato sintasa | citrulina + aspartato | citruliladenilato (citrulil-AMP) |
argininosuccinato |
| activación de ácidos grasos para su β-oxidación | acil-CoA sintetasa | ácido graso + CoA | aciladenilato (acil-AMP) |
acil-CoA |
| activación de aminoácidos para la síntesis proteica | aminoacil-tRNA sintetasa | aminoácido + tRNA | aminoaciladenilato (aminoacil-AMP) |
aminoacil-tRNA |