Nomenclatura de los acilgliceroles y otros glicerolípidos
El glicerol no presenta estereoisomería (no tiene ningún carbono asimétrico
(no tiene ningún carbono asimétrico ) pero es una
molécula proquiral
porque cuando se
esterifican
) pero es una
molécula proquiral
porque cuando se
esterifican los grupos
los grupos
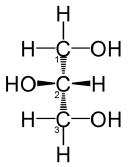 hidroxilo de los carbonos 1
y 3 con distintos sustituyentes el carbono
2 pasa a ser asimétrico. Esto ocurre en distintos derivados
del glicerol como los acilgliceroles y, en estos casos, para denotar de
forma precisa los átomos de carbono del glicerol se utiliza
la numeración
estereoespecífica
(sn
hidroxilo de los carbonos 1
y 3 con distintos sustituyentes el carbono
2 pasa a ser asimétrico. Esto ocurre en distintos derivados
del glicerol como los acilgliceroles y, en estos casos, para denotar de
forma precisa los átomos de carbono del glicerol se utiliza
la numeración
estereoespecífica
(sn ), propuesta
por Hirschmann en 1960, en la que el átomo de carbono del glicerol que
aparece arriba al ser representado en la proyección de
Fischer
), propuesta
por Hirschmann en 1960, en la que el átomo de carbono del glicerol que
aparece arriba al ser representado en la proyección de
Fischer , que muestra
la cadena de carbonos en vertical con el grupo hidroxilo del carbono
central a la izquierda, será el C-1.
, que muestra
la cadena de carbonos en vertical con el grupo hidroxilo del carbono
central a la izquierda, será el C-1.
Según las normas de la IUPAC-IUB de 1976, los
ésteres, éteres y otros O-derivados del glicerol
se denominan utilizando un prefijo para denotar el
sustituyente
que va precedido por su localización numérica. Por
ejemplo, el glicerol esterificado con tres moléculas de
ácido esteárico (18:0) sería: 1,2,3-triestearoilglicerol
(o triestearato de glicerol) en su denominación
común pero 1,2,3-trioctadecanoil-sn-glicerol en la
sistemática.
de 1976, los
ésteres, éteres y otros O-derivados del glicerol
se denominan utilizando un prefijo para denotar el
sustituyente
que va precedido por su localización numérica. Por
ejemplo, el glicerol esterificado con tres moléculas de
ácido esteárico (18:0) sería: 1,2,3-triestearoilglicerol
(o triestearato de glicerol) en su denominación
común pero 1,2,3-trioctadecanoil-sn-glicerol en la
sistemática.
El prefjio 'rac'
(de racemato ) precederá
al nombre si el producto es una mezcla
con cantidades equivalentes de
las dos configuraciones posibles del glicerol; el prefijo 'X'
se utiliza si la configuración del compuesto no se
especifica o no se conoce. Se puede omitir el
localizante 'O'
si la sustitución es en los átomos de
oxígeno del glicerol.
) precederá
al nombre si el producto es una mezcla
con cantidades equivalentes de
las dos configuraciones posibles del glicerol; el prefijo 'X'
se utiliza si la configuración del compuesto no se
especifica o no se conoce. Se puede omitir el
localizante 'O'
si la sustitución es en los átomos de
oxígeno del glicerol.
Ejemplos de nomenclatura:
|
1-O-octil-sn-glicerol
(1-octil-sn-glicerol) |
 |
|
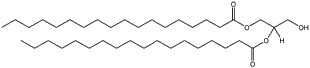
1,2-dioctadecanoil-rac-glicerol |
 |
|
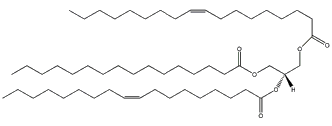
1-hexadecanoil-2,3-di-(9Z-octadecenoil)-sn-glicerol |
 |
De las pautas
de Fahy y col. (2005 y
2009) para la nomenclatura de lípidos se pueden aplicar
a glicerolípidos y
glicerofosfolípidos las normas a), f), g) y h).
Cita:
Hirschmann, H.
(1960) The nature of substrate asymmetry in stereoselective reactions.
J. Biol. Chem. 235, 2762-7.
 ) pero es una
molécula proquiral
porque cuando se
esterifican
) pero es una
molécula proquiral
porque cuando se
esterifican hidroxilo de los carbonos 1
y 3 con distintos sustituyentes el carbono
2 pasa a ser asimétrico. Esto ocurre en distintos derivados
del glicerol como los acilgliceroles y, en estos casos, para denotar de
forma precisa los átomos de carbono del glicerol se utiliza
la numeración
estereoespecífica
(sn
hidroxilo de los carbonos 1
y 3 con distintos sustituyentes el carbono
2 pasa a ser asimétrico. Esto ocurre en distintos derivados
del glicerol como los acilgliceroles y, en estos casos, para denotar de
forma precisa los átomos de carbono del glicerol se utiliza
la numeración
estereoespecífica
(sn ), propuesta
por Hirschmann en 1960, en la que el átomo de carbono del glicerol que
aparece arriba al ser representado en la proyección de
Fischer
), propuesta
por Hirschmann en 1960, en la que el átomo de carbono del glicerol que
aparece arriba al ser representado en la proyección de
Fischer , que muestra
la cadena de carbonos en vertical con el grupo hidroxilo del carbono
central a la izquierda, será el C-1.
, que muestra
la cadena de carbonos en vertical con el grupo hidroxilo del carbono
central a la izquierda, será el C-1.
