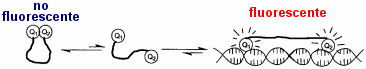
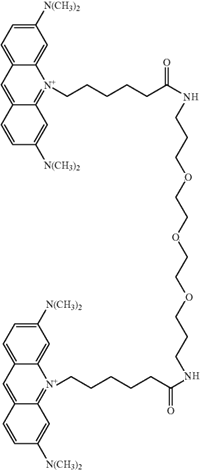
Es el nombre común de tris(hidroximetil) aminometano. Se trata de un compuesto muy utilizado en el laboratorio para preparar disoluciones tampón; el grupo ácido-base que ejerce el tamponamiento es el amino. Se comercializa en sus formas básica ("Tris base") y ácida ("Tris hidrocloruro"), aunque la primera es la de uso más común. Un tampón denominado "Tris-HCl" se prepara con Tris base a la concentración indicada y con el HCl necesario para ajustar el pH al valor indicado. En la electroforesis, es el agente tamponante que mantiene el pH. |
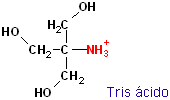 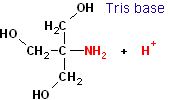
(HOCH2)3C-NH2 Mr ≈ 121 g/mol |